
Alors que l’Europe subit les bombes allemandes, c’est un tout autre type de bombardement que les chercheurs réalisent aux Etats-Unis. Entre intuitions improbables et catastrophe évitée, le carbone 14 se dévoile.
1936, L’intuition de la production du carbone 14
En 1936, Edwin McMillan (1907-1991) remarque la présence d’activités de très longue durée de vie dans d’anciennes cibles de cyclotron et dans des fragments de métal prélevés dans différentes parties de la chambre d’accélération. Il suppose que ces activités peuvent être dues à des espèces radioactives de béryllium et de carbone. Dans un résumé présenté à une réunion de la Physical Society en 1936, il décrit deux activités résiduelles dans une ancienne cible de béryllium. L’activité principale présente un taux de décroissance compatible avec une demi-vie de 10 ans ou plus. Cette composante, pense-t-il, pourrait être provisoirement attribuée au béryllium 10. Il suggère que l’autre activité, de plus faible intensité a une demi-vie de quelques mois, et est attribuable à un isotope radioactif du carbone, en particulier le carbone 14. Edwin McMillan sera prix Nobel de chimie 1951, pas pour cette intuition géniale qui va mettre sur la piste d’une production du carbone 14 insoupçonnée, mais pour ses travaux sur les éléments transuraniens.

A la fin des années 30, les techniques de production et de détection s’améliorent rapidement. En parallèle, l’étude des radio-isotopes occupe de plus en plus de physiciens. Ainsi, en 1939, le fraichement nobélisé de physique Ernest Lawrence (1901-1958), « pour l’invention et le développement du cyclotron et pour les résultats obtenus avec cet instrument, spécialement ceux qui concernent la production d’éléments radioactifs artificiels », demande à Martin Kamen (1913-2002), jeune chimiste spécialisé dans les radio-isotopes, et Samuel Ruben (1913-1943) qui étudie le potentiel de traceurs isotopiques comme le phosphore, le sodium ou l’iode, d’organiser une campagne complète et systématique pour les éléments de la première période du tableau périodique afin de déterminer l’existence d’isotopes à longue durée de vie, notamment l’hydrogène, le carbone, l’azote et l’oxygène.

Kamen et Ruben élaborent un plan détaillé comprenant les protocoles pour chaque réaction nucléaire possible avec les projectiles disponibles, ainsi que le choix des matériaux et des cibles. Ils explorent[1] ensemble la désintégration du carbone 14 et en 1940, ils suggèrent les premiers une durée de vie qui s’étend sur plusieurs années, pressentant le potentiel de cette découverte :
« Le radiocarbone à longue durée de vie sera d’une grande importance pour de nombreuses expériences chimiques, biologiques et industrielles. Bien que le rayonnement émis soit de faible intensité, il peut néanmoins être utilisé pour des analyses quantitatives. »
1940, Les bombardements de l’hiver
Alors que l’Europe subit les bombes allemandes, c’est un tout autre type de bombardement que les chercheurs réalisent aux Etats-Unis.
Martin Kamen expose en continu pendant près d’un mois, en janvier 1940, une cible en graphite, composée majoritairement de carbone 12, à l’intérieur d’un cyclotron, un accélérateur de particules, cette cible est utilisée pour collecter les deutérons[2] parasites du faisceau interne du cyclotron. La sonde est insérée de manière à intercepter la quasi-totalité des deutérons pendant les opérations nocturnes et est ensuite retirée le jour pour permettre un fonctionnement normal, car le cyclotron est particulièrement utilisée pour l’étude de la fission de l’uranium qui vient d’être découverte en Allemagne par Otto Hahn et Fritz Strassmann. La cible n’est pas conçue pour résister à un bombardement intense et Kamen raconte[3] :
« Le temps était exceptionnellement violent, même pour un mois de janvier, et la plupart des nuits étaient marquées par des pluies torrentielles et des tempêtes de vent. Le bruit de la pluie sur le toit en tôle du laboratoire, accompagné des détonations des décharges à haute tension du cyclotron, composait une fanfare appropriée pour la naissance du carbone 14, qui devait se produire lors de ce bombardement. »

co-découvreur du carbone 14
Le 15 février, lors d’un orage particulièrement violent, Kamen met fin à ce bombardement. Peu avant l’aube, il dépose le graphite, qui ressemble à des cailloux, dans un flacon de pesée sur le bureau de Samuel Ruben. Le lendemain, Kamen téléphone à Ruben, qui a brûlé l’échantillon jusqu’à l’obtention de dioxyde de carbone CO₂. Ensuite, il fait précipiter le gaz sous forme de carbonate de calcium CaCO₃ et il constate une certaine activité, certes très faible, environ quatre fois au-dessus du bruit de fond. Convaincus qu’ils viennent de détecter la radioactivité d’un isotope du carbone, les expériences et les analyses se poursuivent au cours du mois de février afin de s’assurer qu’aucune activité parasite ne provienne d’un autre élément. Kamen et Ruben rédigent un compte rendu préliminaire, d’abord sous forme de lettre, puis de résumé, pour une publication dans Physical Review[4]. La voie de production suit alors la chaîne suivante :
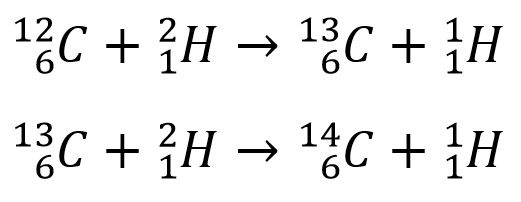
Kamen estime rapidement le temps de demi-vie du carbone 14 dont la formation ne fait plus de doute. Il trouve un temps de demi-vie d’environ 4000 ans, valeur remarquablement proche de la demi-vie réelle de désintégration qui est de 5700 ans, et qui sera déterminée précisément bien plus tard.
1940, La catastrophe évitée de justesse
Kamen et Ruben ont produit du carbone 14 à partir de carbone 12 au prix d’un bombardement intense et coûteux en énergie, mais les premières expériences[5] menées par le physicien anglais Norman Feather (1904-1918) et en 1934 par l’américain Franz Kurie (1907-1972) [6] en 1934, montraient que le carbone 14 pouvait être obtenu par bombardement de neutrons sur de l’azote 14.
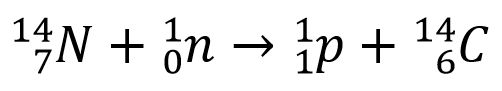
Cette voie avait été abandonnée car on estimait la section efficace des atomes d’azote trop faible et donc l’opération se révélait faiblement rentable.
En janvier 1940, deux bonbonnes contenant chacune 5 gallons (un peu plus de 18L) de solution saturée de nitrate d’ammonium acidifiée NH4NO3, un réactif hautement explosif, sont placées près d’une source importante de neutrons. Une équipe de cyclotron doit régulièrement accéder à un boitier de commande d’un déflecteur, déflecteur qui doit être réglé constamment, or le boitier est imbibé d’acide du fait de la proximité des bonbonnes qui fuient. L’équipe, furieuse, exige que les bonbonnes soient retirées.
Kamen transporte donc les bonbonnes dans le laboratoire de Ruben, surnommé le « Rat House », la maison des rats, et ils décident d’analyser le contenu des bonbonnes. Ils aspirent l’air restant et font précipiter l’éventuel dioxyde de carbone qui serait présent. A leur surprise, ils obtiennent une grande quantité de précipité de carbonate de calcium CaCO3. Dans un premier temps, les deux compères ne sont pas rassurés car cela signifie que de grandes quantités de dioxyde de carbone CO2 ont diffusé dans les solutions de nitrate d’ammonium et que toute activité radioactive formée a probablement été perdue en raison d’une dilution excessive. Mais, ô surprise, ils constatent qu’une petite fraction de ce précipité est si active qu’elle sature complètement leur compteur d’activité ! Ils détectent plusieurs microcuries de carbone 14, une quantité deux à trois ordres de grandeur supérieure à celles obtenues par bombardement des cibles en graphite. Ils comprennent rapidement que le bombardement neutronique d’azote 14 est à l’origine de la production de carbone 14. L’intérêt pour la réaction de formation à partir du carbone 13 cesse et la voie de production par l’azote 14 est privilégiée.

La suite vers la datation au carbone 14, c’est une autre histoire.
[1] Ruben, Samuel, and Martin D. Kamen. “Radioactive Carbon of Long Half-Life.” Physical Review 57, no. 6 (1940): 549–549. https://doi.org/10.1103/physrev.57.549
[2] Un isotope de l’hydrogène, contenant un proton et un neutron.
[3] Kamen Martin D., « Early History of Carbon-14: Discovery of this supremely important tracer was expected in the physical sense but not in the chemical sense« . Science. 140 (3567), 584–590. https://doi.org/10.1126/science.140.3567.584
[4] Ruben Samuel, and Martin D. Kamen. “Radioactive Carbon of Long Half-Life.” Physical Review 57, no. 6 (1940): 549–549. https://doi.org/10.1103/physrev.57.549
[5] Feather Norman, “The Collisions of Neutrons with Nitrogen Nuclei.” Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character 136, no. 830 (1932): 709–27. http://www.jstor.org/stable/95817
[6] Kurie Franz N. D., “A New Mode of Disintegration Induced by Neutrons”, Physical Review, 45, 904 (1934); 46, 330 (1934).
https://doi.org/10.1103/PhysRev.45.904
L’image en avant a été générée par IA.
Les autres images sont issues de Wikipedia.

Laisser un commentaire